Алкоксиглицериды при хроническом стрессе
Введение
С момента своего первого знакомства до настоящего времени проблема стресса и адаптации к стрессу не утратила своей актуальности. Социально-бытовая среда современной жизни создает у подавляющего большинства людей длительное, постоянное психоэмоциональное напряжение. Постоянные психические и психоэмоциональные нагрузки, нарушение режима труда, отдыха и питания нередко приводят к срыву механизмов адаптации и развитию заболеваний. Селье [ 1] приводится длинный список болезней адаптации, в который входят болезни сердечно-сосудистой системы (такие как болезни сердца, гипертония, гипотония, атеросклероз и др.), нервной системы (например, психосоматические расстройства, неврозы, неврастения, психозы), желудочно-кишечного тракта (в частности, язвы желудочно-кишечного тракта и язвенный колит), анемии и другие расстройства.
Все больше и больше веществ исследуются в качестве потенциального средства для уменьшения стресса и его последствий. Цель нашей работы – определить, является ли применение АГ эффективным методом лечения хронического стресса.
АГ являются предшественниками таких биологически активных веществ, как плазмалогены и фактор активации тромбоцитов (ФАТ). ФАТ является мощным биорегулятором с широким спектром физиологических функций. PAF привлек большое внимание как универсальный медиатор воспаления, продуцируемый различными типами иммунных клеток, в частности нейтрофилами, эозинофилами и макрофагами, а также эндотелиальными клетками и тромбоцитами [2 ] .
Плазмалогены представляют собой класс мембранных глицерофосфолипидов с уникальными свойствами. Плазмалогены имеют решающее значение для здоровья человека; они важны для развития нейронов, для иммунного ответа и в качестве эндогенных антиоксидантов. Учитывая обилие и распределение плазмалогенов во многих мембранных системах и в различных тканях, неудивительно, что плазмалогены играют ключевую роль во многих биологических функциях [ 2 , 3 , 4 ]. Появляется все больше доказательств терапевтического потенциала модуляции уровней плазмалогена для предотвращения или лечения кардиометаболических и нейродегенеративных заболеваний [ 3 , 4 ].
Ранее нашим коллективом было проведено исследование влияния АГ при водно-иммобилизационном стрессе, выявившее их положительный эффект [ 5 ]. Это исследование стало отправной точкой для нашего интереса к этой проблеме. Других работ по изучению АГ в стрессовых условиях нет.
Результаты
2.1. Изменения массы тела у крыс, получавших АГ.
На предварительном этапе эксперимента (обработка АГ до начала стрессорного воздействия) достоверных различий (t = 0,3; p = 0,76) в общей прибавке массы тела между животными, получавшими АГ, не было (общая прибавка массы тела 23,2). ± 5,6%) и животных контрольной группы (общая прибавка массы тела 22,5 ± 4%) ( рис. 1 ).
Маринедракс 21 00202 g001 550
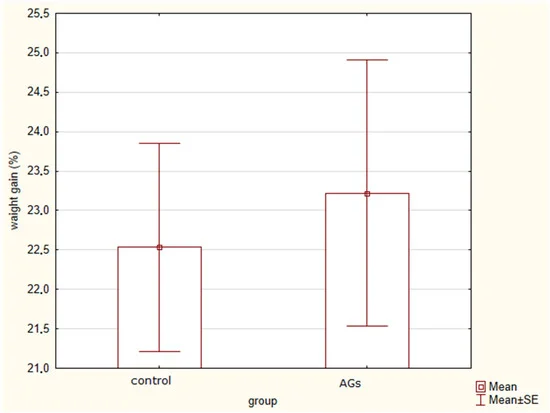
Рисунок 1. Общее увеличение массы тела у крыс, получавших АГ, без существенных различий.
2.2. Изменения массы тела при стрессе
Достоверные различия в приросте массы тела были обнаружены после первой недели стресса (Н = 9,0; р = 0,01), а также в конце эксперимента (Н = 9,3; р = 0,01). Стресс ожидаемо снижал массу тела с самым сильным эффектом в первую неделю (см. Приложение А и Приложение Б ). На второй и третьей неделе стресса различия в приросте массы тела между стрессированными животными и животными, получавшими АГ на фоне стресса и без него, уже не были достоверными.
2.3. Содержание липопротеидов в сыворотке крови
В таблице 1 представлены параметры липидного обмена у крыс после окончания эксперимента. Дисперсионный анализ (H = 9,24; p = 0,0262) выявил различия между группами в концентрациях триглицеридов ( рис. 2 ). Лечение стрессом и АГ приводит к снижению уровня триглицеридов. Существовали достоверные различия между контрольными крысами и стрессированными животными (t = 2,7, p = 0,03), а также между крысами, получавшими АГ и подвергнутыми стрессу (t = 2,9, p = 0,02), но не между контрольной группой и контрольной группой. группа, получавшая АГ (t = 1,33; p = 0,22), или между животными, подвергшимися стрессу, и животными, получавшими АГ до стресса (t = -0,1; p = 0,91).
Маринедракс 21 00202 g002 550
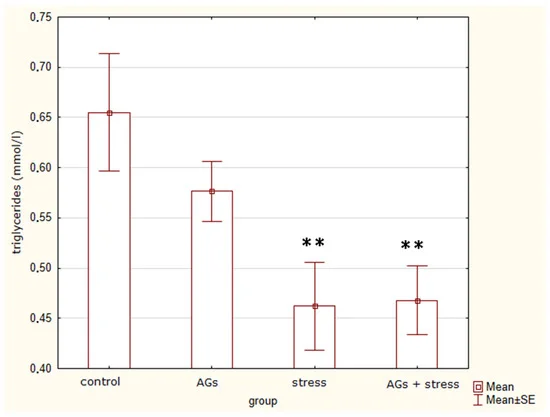
Рис. 2. Концентрация триглицеридов, указывающая на статистически значимые различия между контрольной и опытной группами: ** p < 0,05.
| Индикатор | Контроль | АГ | стресс | АГ + стресс | |
|---|---|---|---|---|---|
| Общий холестерин, ммоль/л | 1,8 1,4–2,05 | 1,6 1,2–1,6 | 1,4 1,2–1,5 | 1,1 1,1–1,4 | Н = 6,64 ′ р = 0,08 |
| ХС-ЛПВП, ммоль/л | 0,88 ± 0,16 | 0,98 ± 0,16 | 0,93 ± 0,16 | 0,9 + 0,19 | F = 0,34″ p = 0,79 |
| Хс-ЛПНП, ммоль/л | 0,55 0,24–0,85 | 0,18 0,1–0,45 | 0,15 0,06–0,26 | 0,1 0,05–0,11 | Н = 3,84 р = 0,28 |
| ХС ЛПОНП, ммоль/л | 0,3 ± 0,05 | 0,26 ± 0,03 | 0,21 ± 0,04** | 0,21 ± 0,04** | F = 4,9 р = 0,013 * |
| Коэффициент атерогенности | 0,89 0,65–1,34 | 0,43 0,36–0,7 | 0,34 0,33–0,56 | 0,45 0,22–0,47 | Н = 4,45 р = 0,22 |
| Триглицериды, ммоль/л | 0,66 ± 0,12 | 0,58 ± 0,07 | 0,46 ± 0,1** | 0,47 ± 0,08** | F = 4,8 р = 0,014 * |
Таблица 1. Показатели липидного обмена.
Кроме того, с помощью дисперсионного анализа мы определили различия (H = 9,68; p = 0,0215) среди крыс в концентрации ЛПОНП-Х ( рис. 3 ). Воздействие стресса (t = 2,69, p = 0,03) и стресса с АГ (t = 2,96, p = 0,02) приводит к снижению уровня ХС ЛПОНП. Лечение АГ снижало уровень ХС ЛПОНП, но незначительно (t = 1,31, p = 0,23) по сравнению с контрольной группой. Кроме того, лечение АГ до стресса лишь незначительно повышало уровни ЛПОНП-Х (t = 2,0, p = 0,1). Таким образом, только стресс значительно влиял на уровень холестерина ЛПОНП.
Маринедракс 21 00202 g003 550
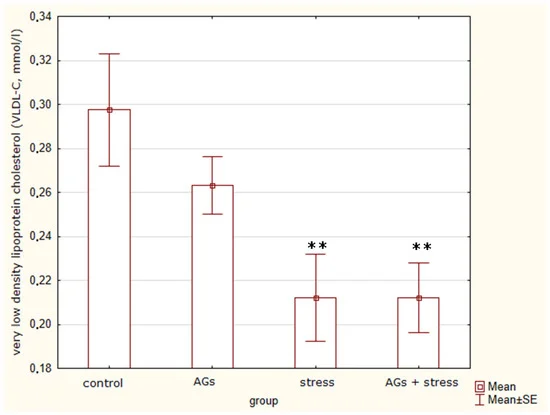
Рис. 3. Концентрация холестерина липопротеинов очень низкой плотности, указывающая на статистически значимые различия между контрольной и экспериментальной группами: ** p < 0,05.
Таким образом, количество ЛПОНП-Х и триглицеридов в крови достоверно снижалось при стрессе.
2.4. Влияние АГ на содержание и состав жирных кислот и уровень плазмалогена в липидах плазмы
Жирнокислотный состав общих липидов плазмы крыс представлен в Приложении С. Существенных различий в составе основных жирных кислот не обнаружено. На рис. 4 показано изменение уровня плазмалогенов в соотношении 16:0 ДМА/16:0 МЭЖК в опытных группах. Под действием АГ ( р < 0,05) концентрация 16:0 ДМА повышалась в группах с пероральным введением АГ по сравнению с контрольными животными.
Маринедракс 21 00202 g004 550
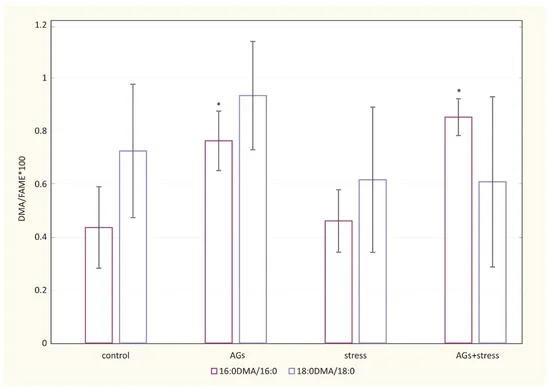
Рис. 4. Влияние АГ на липиды плазмы крови крыс контрольной и экспериментальной групп. Относительное количество плазмалогена отражалось в соотношении 18:0 диметилацеталя (ДМА) (% от суммы МЭЖК и ДМА) к стеариновой кислоте (% от суммы МЭЖК и ДМА), а также в соотношении 16:0 DMA (% от общего количества FAME и DMA) до пальмитиновой кислоты (% от общего количества FAME и DMA). * Статистически значимые различия между контрольной и опытной группами: * p < 0,05.
2.5. Результаты анализа крови
Гематологические показатели клинических анализов крови животных приведены в Приложении D. Достоверных различий между группами по количеству эритроцитов (Н=2,07; р =0,56), уровню гематокрита (Н=1,63; р =0,65) и количеству гемоглобина (Н=4,02; р =0,26) не выявлено. ).
Существовала значительная разница между группами по процентному содержанию лимфоцитов (H = 8,49; p = 0,037). Тест Манна-Уитни выявил различия между контрольной группой и животными, получавшими АГ на фоне стресса (Z = -2,08; p = 0,03), а также между группой стресс-контроль и животными, получавшими АГ на фоне стресса. (Z = -2,33; р = 0,016). Так, процентное содержание лимфоцитов снижалось при стрессовом воздействии и, наоборот, повышалось в группе стресса, получавшей АГ.
Маринедракс 21 00202 g005 550
Соотношение нейтрофилов и лимфоцитов также различалось между группами (H = 9,15; p = 0,0273) ( рис. 6 ). У животных, подвергшихся хроническому стрессу, соотношение было выше, чем в группе, получавшей АГ на фоне стресса (Z = 2,33; p = 0,016), и выше, чем в контрольной группе.
Маринедракс 21 00202 g006 550
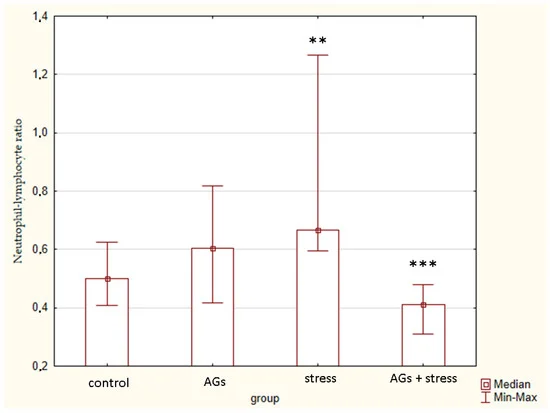
Рис. 6. Соотношение нейтрофилов и лимфоцитов, указывающее на статистически значимые различия в контрольной группе ** и группе стресса *** p < 0,05.
Тест Краскела-Уоллиса не выявил достоверных различий между группами, исходя из показателей массы селезенки (H = 1,65 p = 0,65), тимуса (H = 2,63 p = 0,45) и надпочечников (H = 3,11; p = 0,38).
2.7. Уровни гормонов
Уровни тестостерона (H = 0,79; p = 0,85) и кортизола (H = 3,79; p = 0,28).
Достоверных различий в уровнях этих гормонов между группами не было. Тем не менее максимальный уровень тестостерона определялся у животных, получавших АГ.
Обсуждение
Иммобилизация обычно широко используется в качестве стрессора для изучения связанных со стрессом биологических, биохимических и физиологических реакций у животных. Иммобилизацию можно производить двумя различными способами. Животных можно держать обездвиженными в полуцилиндрической акриловой трубе с соответствующими отверстиями для прохождения воздуха, или животных можно растянуть на доске с иммобилизованными конечностями с помощью липкой ленты. Во втором случае движения головы ограничиваются металлической петлей, намотанной на шею [ 6 ]. Существуют также различные режимы иммобилизации, подробно описанные в современной литературе. Для исследования мы выбрали классическую модель напряжений [ 7 , 8 , 9 ] .]. Даже простой эмоциональный стресс может привести к серьезной тревожной реакции. Нервные волнения чрезвычайно эффективны в качестве тревожных раздражителей. Благодаря своему сложному разветвлению нервная система легко передает импульсы ко многим частям тела, и если эти раздражители сильны, они вызывают системный стресс [ 1 ].
АГ в выбранной дозе не оказывают значимого влияния на общую прибавку массы тела крыс через 1,5 мес применения. Согласно литературным данным, высокие дозы селахилового спирта снижали массу тела, уровень триглицеридов в сыворотке, уровень холестерина, уровни глюкозы натощак, уровни инсулина и уровни лептина в сыворотке у мышей, получавших диету с высоким содержанием жиров, в то время как высокие дозы батилового спирта увеличивали уровни инсулина у мышей, получавших диету с высоким содержанием жиров [ 10 ].
Во время эксперимента образцы селезенки хранились. Затем часть образцов использовали для оценки уровня плазмалогенов в этом органе. Сделан вывод о слабом влиянии селезенки при хроническом иммобилизационном стрессе; колебания содержания жирных кислот были незначительными. Таким образом, не выявлено влияния АГ на липидный состав селезенки [ 11 ].
Хронический стресс приводил к снижению массы тела животных в течение первой недели. Таким образом, наиболее значимое влияние стресса наблюдалось в первую неделю иммобилизации. Отсутствие значимых изменений массы тимуса, надпочечников и селезенки свидетельствует о развитии резистентной стадии. На это также указывает отсутствие выраженных различий в уровне кортизола. Кроме того, по данным литературы, повышение уровня кортикостерона характеризует острый, а не хронический гомотипический стресс [ 7 , 12 ].
Некоторыми очень важными данными нашего исследования являются процентное содержание лимфоцитов и соотношение нейтрофилов и лимфоцитов. Повышенное соотношение нейтрофилов и лимфоцитов было связано с воздействием хронического стресса [ 12 ]. На основании уровней кортизола и соотношений нейтрофилов и лимфоцитов вместе можно сделать вывод об успешной реализации модели хронического иммобилизационного стресса.
Увеличение процентного содержания лимфоцитов в стрессовой группе животных при лечении АГ согласуется с литературными данными. АГ могут модулировать иммунный ответ, усиливая пролиферацию и созревание мышиных лимфоцитов in vitro [ 13 ]. У мышей с дефицитом пероксисомального фермента глицеронфосфат-О-ацилтрансферазы (GNPAT), необходимого для синтеза эфирных липидов, наблюдалось значительное изменение созревания iNKT-клеток в тимусе и меньшее количество iNKT-клеток как в тимусе, так и в периферических органах [14 ] . Масло печени акулы способно увеличивать пролиферацию лимфоцитов у крыс [ 15 ], лейкоцитов, лимфоцитов, нейтрофилов, моноцитов и уровень IgG в крови поросят от свиноматок, получающих добавки [ 16 ].]. Лейкоциты, IgG и лимфоциты достоверно повышались, тогда как нейтрофилы значительно снижались у стареющих пациентов после хирургического лечения благодаря АГ в дозе 500 мг 2 раза в сутки в течение 4 нед [17 ] . Таким образом, можно заключить, что АГ оказывают опосредованное влияние на клетки крови [ 18 ].
Увеличение процентного содержания лимфоцитов в стрессовой группе животных под влиянием АГ мы рассматриваем как положительный признак, так как длительное угнетение иммунитета при хроническом стрессе неблагоприятно для организма. Было показано, что восстановление уровня плазмалогена с помощью заместительной терапии плазмалогеном является успешной противовоспалительной стратегией [ 19 ]. Следовательно, животные, получавшие АГ, лучше переносили хронический стресс.
Таким образом, АГ обладают некоторыми полезными свойствами как при остром [ 5 ], так и при хроническом стрессе.
Материалы и методы
4.1. Животные
Исследование проведено на 32 крысах-самцах линии Вистар (по 8 в каждой группе) в течение 2 мес. Животных содержали в виварии, на стандартном рационе без каких-либо добавок, со свободным доступом к пище и воде. Средняя масса животных в начале опыта составляла 171 ± 19 г. Все процедуры были одобрены Комитетом по этике животных Национального научного центра биологии моря им. А.В. Зирмунского (ДВО РАН, Владивосток, Россия) в соответствии с Руководством по благополучию лабораторных животных.
4.2. Подготовка
4.2.1. Подготовка АГ
Кальмар Berryteuthis magister был пойман в Беринговом море за год до нашего эксперимента. После обработки кальмаров печень удаляли и хранили в течение 3 месяцев при -18°С. Все химические реагенты, использованные в этом исследовании, имеют аналитическую чистоту (Sigma-Aldrich, Сент-Луис, Миссури, США). Все растворители имели квалификацию для ВЭЖХ, поставлялись Sigma-Aldrich (США).
Экстракцию общих липидов проводили по Блаю и Дайеру [ 20 ]. Омыление липидов проводили по методике, описанной Кристи [ 21 ].
Осаждение АГ из омыленных липидов проводили методом двойной кристаллизации в ацетоне при разных температурах [ 22 ]. Количество АГ в смеси определяли методом ГХ с использованием стандарта АГ-С8:0 и с помощью ТСХ по методике [ 22 ]. Окончательная форма используется в дополнении «НаноРазум» (Москва, Россия).
4.2.2. Определение состава АГ
Состав АГ в виде ТМС-АГ определяли методами ГХ и ГХ-МС.
ТМС-АГ готовили следующим образом: объем 50 мкл N , O-Бис(триметилсилил)-трифторацетамид добавляли к 5 мг АГ; смесь нагревали до 80°C в течение 1 часа. После добавления 200 мкл гексана в ГХ вводили по 1 мкл каждой силилированной фракции. Состав ТМС-АГ определяли методом ГХ с использованием хроматографа Shimadzu GC-2010 Plus с пламенно-ионизационным детектором (Kyoto, Япония) и капиллярной колонки Supelco SLB™-5 ms, 30 м × 0,25 мм ID (США). Разделение компонентов смеси проводили при следующих условиях: начальная температура 200 °С и скорость нагрева 2 °С/мин до 290 °С. Температуру поддерживали в течение 35 мин. Температура инжектора составляла 270 °С, а температура детектора — 250 °С. Идентификацию АГ проводили путем сравнения с доступными известными стандартами. ГХ-МС использовали для идентификации структуры ТМС-АГ.
Состав осажденной насыщенной фракции АГ приведен в табл. 4 , а изображение химической структуры — на рис. 7 .
Маринедракс 21 00202 g007 550
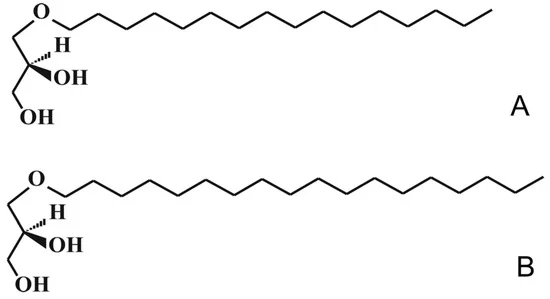
Рисунок 7. Химическая структура алкилглицеролов. ( А ) – химиловый спирт, ( Б ) – батиловый спирт.
Несмотря на то, что содержание ненасыщенных АГ в исходных гидролизатах липидов составляло 17,5% (от общего количества АГ), полученный препарат содержал только насыщенные радикалы.
Полученный препарат АГ представлял собой белый рассыпчатый порошок без запаха.
4.3. Биологический эксперимент
4.3.1. Лечение животных
Мы использовали препарат 99% АГ с химическим содержанием спирта (радикал 16,0), который составлял 95% от общего количества АГ ( таблица 4 и рисунок 7 ). АГ, предназначенные для животных, диспергировали в воде. Крысы получали лекарство или воду перорально через катетер в течение шести недель (1,5 месяца).
Экспериментальные группы (по восемь животных в каждой):
1 группа – животные получали воду (контроль);
2-я группа — животные получали АГ в дозе 200 мг/кг массы тела;
3 группа – животные получали воду и подвергались стрессу (стресс-контроль);
4 группа — животные получали АГ в дозе 200 мг/кг и подвергались стрессу.
Введение через зонд различных носителей может привести к аспирации, повреждению легких и/или возникновению стрессовой реакции в зависимости от объема носителя и дозы. Объемы дозы для введения крысам через желудочный зонд обычно не должны превышать 10 мл/кг. Введение через зонд кукурузного масла в дозе ≥20 мл/кг, но не 1% метилцеллюлозы/0,2% Tween 80 или воды, вызывало стрессовую реакцию в зависимости от объема, что приводило к повышению уровня кортикостерона в плазме [23 ] . В нашем исследовании объем вводимого вещества не превышал 2 мл/кг. Поэтому мы предполагаем, что данная манипуляция не привела к существенному отклонению в состоянии животных в нашем исследовании, поэтому мы не вводили в исследование дополнительную интактную контрольную группу.
4.3.2. Стресс-процедура
Хронический иммобилизационный стресс [ 6 ] вызывали у крыс путем помещения животных в индивидуальные плексигласовые футляры с отверстиями для вентиляции на 2 ч [ 7 ] ежедневно в течение 15 дней [ 8 ]. Схема имеет аналоги в литературе [ 9 ].
4.3.3. Измерение массы тела
В ходе эксперимента животных взвешивали на электронных весах с интервалом 5–10 дней.
Общий прирост массы тела при лечении АГ до стресса, общий прирост массы тела при стрессовом воздействии и прирост массы тела в течение каждой недели стресса рассчитывали следующим образом:
Прибавка в весе (%) = (W1 − W0)/W0
начальная прибавка в весе (W0)
новая прибавка в весе (П1)
4.3.4. Сбор образцов
Крыс анестезировали изофлураном и умерщвляли декапитацией. Кровь для биохимических и гематологических исследований брали при декапитации.
Взвешивали надпочечники, селезенку и тимус.
4.3.5. Липидный спектр сыворотки крыс
Липидный спектр сыворотки крови оценивали по содержанию общего холестерина (ОХ), триглицеридов (ТГ), холестерина липопротеинов высокой плотности (ХС ЛПВП), холестерина липопротеинов низкой плотности (ХС ЛПНП) и холестерина очень низкой плотности (ХС ЛПОНП). ). Концентрацию ОХ и ТГ определяли ферментативным колориметрическим методом на автоматическом биохимическом анализаторе ChemWell Combo 2910 (Awareness Technology, Палм-Сити, США), а концентрацию ХС-ЛПВП — на биохимическом полуавтоматическом фотометре RIELE 5010V5+ (Riele , Берлин, Германия) с использованием наборов «Олвекс Диагностикум» (Санкт-Петербург, Россия). ХС ЛПНП и ХС ЛПОНП рассчитывали по формуле Фридвальда [ 24 , 25 ] в модификации (см. пример в [ 26 ]).
ХС-ЛПНП = ТС – ХС ЛПОНП – ХС ЛПВП
ЛПОНП-Х = ТГ/2
Результаты выражали в мкм/л.
Коэффициент атерогенности (КА) рассчитывали по формуле [ 27 ]:
AC = (TC – HDL-C) / HDL-C
4.3.6. Содержание жирных кислот и диметилацеталей (ДМА) в общих липидах плазмы крови крыс.
Липиды из плазмы крыс экстрагировали по методу Блая и Дайера, 1957 г. [ 20 ]. Метиловые эфиры жирных кислот (МЭЖК) и ДМА из липидов печени крыс получали по методике Carreau and Dubacq, 1978 [ 28 ]. α,β-ненасыщенный эфир в молекуле плазмалогена в процессе переэтерификации превращался в ДМА соответствующего альдегида, и, таким образом, относительное количество плазмалогена отражалось в соотношении 18:0 альдегида и стеариновой кислоты, а также в соотношении между 16:0 альдегидом и пальмитиновой кислотой согласно Bjorkhem et al., 1986 [ 29]. Анализ МЭЖК и ДМА проводили методом ГХ на хроматографе Shimadzu GC-17A (Shimadzu) с пламенно-ионизационным детектором и капиллярной колонкой 30 м × 0,25 мм, id Supelcowax 10 (Bellefonte). Анализ проводили при следующих условиях: температура колонки 190 °С, температура инжектора и детектора 240 °С. В качестве газа-носителя использовался гелий. Пики метиловых эфиров жирных кислот идентифицировали по временам удерживания отдельных эфиров ЖК путем сравнения их эквивалентных чисел длины углерода с аутентичными стандартами (смесь ПНЖК-3 из менхаденового масла была приобретена у Supelco). Идентификацию DMA проводили путем сравнения времени удерживания со стандартами 16:0 DMA и 18:0 DMA (Sigma-Aldrich).
4.3.7. Гормональные исследования
Уровни кортизола и тестостерона в плазме крови определяли иммуноферментным методом с использованием наборов «Вектор» (Новосибирск, Россия) по методике производителя.
4.3.8. Гематологический анализ
Гематологические показатели периферической крови, в том числе гематокрит, тромбокрит, количество эритроцитов, тромбоцитов, лейкоцитов, лимфоцитов, нейтрофилов, эозинофилов, базофилов и моноцитов (МИД), средний объем эритроцитов, коэффициент вариации ряда распределения эритроцитов, стандартное отклонение диапазона распределения эритроцитов, средний объем тромбоцитов и диапазон распределения тромбоцитов, уровень гемоглобина в крови, средняя концентрация гемоглобина в эритроцитах и среднее содержание гемоглобина в одном эритроците оценивали с использованием гематологического анализатора Abacus (Diatron, Medley, FL, USA).
Рассчитывали соотношение нейтрофилов и лимфоцитов [ 12 ].
4.4. Статистический анализ
Тест Шапиро-Уилка использовался для проверки распределения данных. Данные представлены в виде среднего ± стандартное отклонение или в виде медианы, нижнего (25%, Q25) и верхнего (75%, Q75) квартилей. Статистическую обработку данных проводили с помощью программы «Statistica 10.0». Для выявления статистически значимых различий использовали односторонний ANOVA, двусторонний непарный t- критерий Стьюдента, критерий Краскела-Уоллиса и критерий Манна-Уитни. Статистическая вероятность p < 0,05 считалась значимой [ 30 ].
Выводы
АГ предотвращают многие негативные последствия острого и хронического стресса. В частности, они улучшают иммунный статус животных в условиях хронического стресса.
Препараты с участием АГ могут быть полезны в профилактике и лечении социально значимых заболеваний современного мира.
Рекомендации
- Selye, H. Физиология и патология воздействия стресса ; ACTA, Inc.: Монреаль, Квебек, Канада, 1950. [ Google Scholar ]
- Дорнингер, Ф .; Форсс-Петтер, С.; Виммерб, И.; Бергер, Дж. Плазмалогены, фактор активации тромбоцитов и не только – эфирные липиды в передаче сигналов и нейродегенерации. Нейробиол. Дис. 2020 , 145 , 105061. [ Google Scholar ] [ CrossRef ]
- Браверман, штат Небраска; Мозер А.Б. Функции липидов плазмалогена в норме и при патологии. Биохим. Биофиз. Acta 2012 , 1822 , 1442–1452. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Зеленая версия ]
- Пол, С .; Ланкастер, штат Джорджия; Meiklea, PJ Plasmalogens: потенциальная терапевтическая мишень для нейродегенеративных и кардиометаболических заболеваний. прог. Липид Рез. 2019 , 74 , 186–195. [ Академия Google ] [ Перекрестная ссылка ]
- Полещук Т.С.; Султанов, Р.М.; Ермоленко, Е.В.; Шульгина, Л.В.; Касьянов С.П. Защитное действие алкилглицеринов при стрессе. Стресс 2019 , 23 , 213–220. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Бхатия, Н.; Маити, ПП; Чоудхари, А .; Тули, А .; Масих, Д.; Хан, ММУ; Ара Т. Модели животных в изучении стресса: обзор. НШМ Дж. Фарм. Здоровьеc. Управление 2011 , 2 , 42–50. [ Академия Google ]
- Ли, Х.-Дж.; Парк, Х.-Дж.; Старквезер, А .; Ан, К .; Шим И. Снижение высвобождения интерлейкина-4 из нейронов голубого пятна в ответ на иммобилизационный стресс. Медиат. Воспаление. 2016 , 2016 , 3501905. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Green Version ]
- Хужахметова, Л.К.; Теплый Д.Л. Фармакологическая коррекция процессов перекисного окисления липидов и перекисного гемолиза эритроцитов у половозрелых крыс при иммобилизационном стрессе. Нац. науч. 2016 , 2 , 66–71. [ Академия Google ] [ Перекрестная ссылка ]
- Тиан, В .; Аканда, МР; Ислам, А .; Ян, Х.-Д.; Ли, С.-К.; Ли, Дж.-Х.; Ким, С.-К.; Чой, Ю.-Дж.; Им, С.-Ю.; Парк, Б.-Ю. Антистрессовый эффект мяты полевой у обездвиженных крыс. Междунар. Дж. Мол. науч. 2018 , 19 , 355. [ Google Scholar ] [ CrossRef ] [ Зеленая версия ]
- Чжан, М .; Солнце, С .; Тан, Н.; Кай, В .; Qian, L. Пероральное введение алкилглицеролов по-разному модулирует ожирение, вызванное диетой с высоким содержанием жиров, и резистентность к инсулину у мышей. Дополнение, основанное на доказательствах. Альтерн. Мед. 2013 , 2013 , е11. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Перевозников, И.Е.; Полещук Т.С.; Веланский П.В. Влияние хронического иммобилизационного стресса и 1-0- алкилглицеролов на жирнокислотный состав селезенки крыс. В юбилейной международной научной конференции «90 лет — от растения к лекарству: достижения и перспективы» Сборник научных трудов ; ВИЛАР: Москва, Россия, 2021. [ Google Scholar ]
- Лебедь, член парламента; Хикман, Д.Л. Оценка соотношения нейтрофилов и лимфоцитов как показатель дистресса у крыс. Лаборатория Аним. 2014 , 43 , 276–282. [ Академия Google ] [ Перекрестная ссылка ]
- Цянь, Л .; Чжан, М .; Ву, С .; Чжун, Ю .; Ван Тол, Э .; Cai, W. Алкилглицеролы модулируют пролиферацию и дифференцировку неспецифических агонистов и специфических антиген-стимулированных лимфоцитов селезенки. PLoS ONE 2014 , 9 , e96207. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Зеленая версия ]
- Фаччиотти, Ф.; Раманджанеюлу, GS; Лепор, М.; Сансано, С.; Каваллари, М .; Кистовская, М .; Форсс-Петтер, С.; Ни, Г.; Колоне, А .; Сингхал, А .; и другие. Липиды, полученные из пероксисом, представляют собой аутоантигены, которые стимулируют инвариантные Т-клетки естественных киллеров в тимусе. Нац. Иммунол. 2012 , 13 , 474–480. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Виторино, округ Колумбия; Баззачера, CF; Кури, Р.; Фернандес, Л.С. Влияние хронического приема масла печени акулы на иммунные реакции крыс, прошедших тренировку. Евро. Дж. Заявл. Физиол. 2010 , 108 , 1225–1232. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Митре, Р.; Этьен, М .; Мартинайс, С.; Лосось, Х .; Аллауме, П.; Легран, П.; Легран, А.Б. Улучшение гуморальной защиты и стимуляция кроветворения у свиноматок и потомства путем перорального приема масла печени акулы матерями во время беременности и лактации. бр. Дж. Нутр. 2005 , 94 , 753–762. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Зеленая версия ]
- Палмиери, Б.; Пеннелли, А .; Ди Чербо, А. Хирургия юрского периода и повышение иммунитета с помощью алкиглицеролов масла печени акулы. Здоровье липидов Дис. 2014 , 13 , 178. [ Google Scholar ] [ CrossRef ] [ Зеленая версия ]
- Яннитти, Т .; Palmieri, B. Новые сведения о терапевтической роли алкилглицеролов. Mar. Drugs 2010 , 8 , 2267–2300. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Бозелли, Дж. К.; Ажер, С .; Эпанд, Р.М. Плазмалогены и хронические воспалительные заболевания. Передний. Физиол. 2021 , 12 , 730829. [ Google Scholar ] [ CrossRef ]
- Блай, Э.Г.; Dyer, WJ Быстрый метод экстракции и очистки общих липидов. Может. Дж. Биохим. Физиол. 1957 , 37 , 911–917. [ Академия Google ] [ Перекрестная ссылка ]
- Christie, WW Анализ липидов: выделение, разделение, идентификация и структурный анализ липидов ; The Oily Press: Bridgwater, UK, 2003. [ Google Scholar ]
- Ермоленко, Е.В.; Латышев, Н.А.; Султанов, Р.М.; Касьянов С.П. Технологический подход к выделению 1- О -алкил-sn-глицеринов из масла печени кальмара Berryteuthis magister . Дж. Пищевая наука. Технол. 2016 , 53 , 1722–1726. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Браун, АП; Дингер, Н.; Левин, Б.С. Стресс, вызванный введением крыс через желудочный зонд. Контемп. Вершина. лаборатория Аним. науч. 2000 , 39 , 17–21. [ Академия Google ]
- Фридевальд, WT; Леви, Род-Айленд; Фредриксон Д.С. Оценка концентрации холестерина липопротеинов низкой плотности в плазме без использования препаративной ультрацентрифуги. клин. хим. 1972 , 18 , 499–502. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Санчес-Мунис, Ф.Дж.; Bastida, S. Не используйте формулу Фридевальда для расчета холестерина ЛПНП у крыс с гиперхолестеринемией. Евро. J. Науки о липидах. Технол. 2008 , 110 , 295–301. [ Google Scholar ] [ CrossRef ][ Зеленая версия ]
- Чжао, С.-П.; Ли, Р .; Дай, В .; Ю, Б.-Л.; Чен, Л.-З.; Хуан, X.-S. Xuezhikang способствует большему снижению уровня триглицеридов, чем симвастатин, у крыс с гипертриглицеридемией за счет усиления аполипопротеина A5 через сигнальный путь PPARα. PLoS ONE 2017 , 12 , e0184949. [ Google Scholar ] [ CrossRef ] [ PubMed ][ Зеленая версия ]
- Бхардвадж, С.; Бхаттачарджи, Дж.; Бхатнагар, МК; Тьяги, С. Индекс атерогенности плазмы, индекс риска Кастелли и коэффициент атерогенности — новые параметры в оценке сердечно-сосудистого риска. Междунар. Дж. Фарм. биол. науч. 2013 , 3 , 359–364. Доступно в Интернете: www.ijpbs.com (по состоянию на 15 декабря 2022 г.).
- Карро, JP; Дубак, Дж. П. Адаптация метода макромасштаба к микромасштабу для метиловой переэтерификации жирных кислот биологических липидных экстрактов. Ж. Хроматогр. А 1978 , 151 , 384–390. [ Академия Google ] [ Перекрестная ссылка ]
- Бьорхем, И.; Сисфонтес, Л.; Бостром, Б.; Касе, Б.Ф.; Бломстранд, Р. Простая диагностика синдрома Зеллвегера с помощью газожидкостной хроматографии диметилацеталей. Дж. Липид Рез. 1986 , 27 , 786–791. [ Академия Google ] [ Перекрестная ссылка ]
- Шефф, С.В. Фундаментальные статистические принципы для нейробиолога ; Academic Press: Лондон, Великобритания, 2016 г. [ Google Scholar ]
- Отказ от ответственности/Примечание издателя: Заявления, мнения и данные, содержащиеся во всех публикациях, принадлежат исключительно отдельным авторам и участникам, а не MDPI и/или редакторам. MDPI и/или редактор(ы) отказываются от ответственности за любой ущерб людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании.
© 2023 авторами. Лицензиат MDPI, Базель, Швейцария. Эта статья находится в открытом доступе Marine Drugs
